Giriş
İmmünoterapi — vücudun kendi bağışıklık sistemini kanser hücrelerine karşı harekete geçiren tedavi yaklaşımı — onkolojinin hızla gelişen alanlarından biridir.1 Bu yazıda yalnızca resmi kurum sayfaları, regulator onay kayıtları veya PubMed/NIH gibi izlenebilir kaynaklarla doğrulanabilen gelişmeler özetlenir.
Odak noktaları: ameliyat öncesi/sonrası kullanılan perioperatif immünoterapi onayları, cilt altı uygulanabilen yeni formülasyonlar, seçilmiş FDA kararları, Türkiye’de geri ödeme bilgisinin nasıl doğrulanacağı ve araştırma aşamasındaki kişiselleştirilmiş kanser aşılarıdır.
1. Perioperatif İmmünoterapi: Ameliyat Öncesi ve Sonrası Kullanım Genişliyor
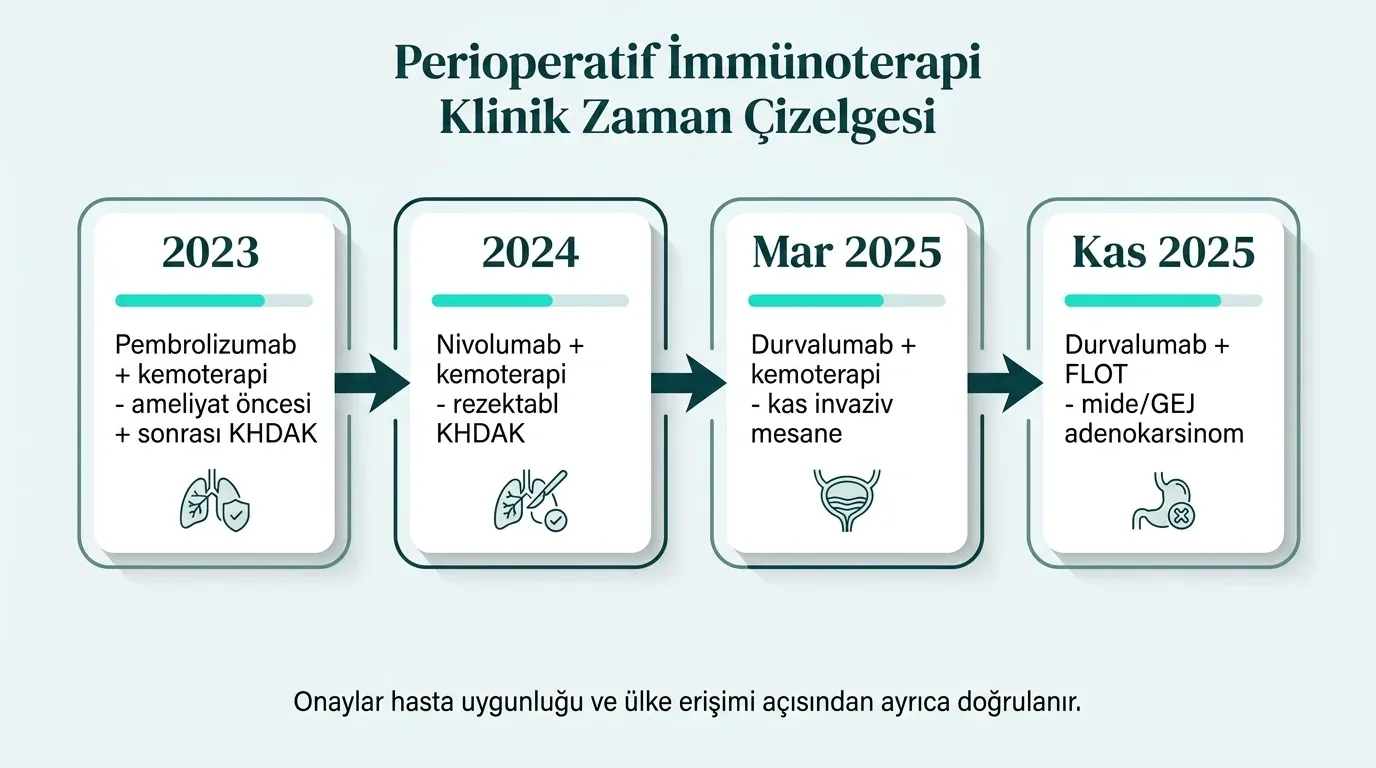
İmmünoterapinin önemli gelişim alanlarından biri perioperatif kullanımdır: bazı ilaçlar yalnızca ileri evrede değil, seçilmiş ameliyat edilebilir tümörlerde ameliyat öncesi (neoadjuvan) ve/veya ameliyat sonrası (adjuvan) dönemde de değerlendirilmektedir.2, 3, 4, 5
Akciğer kanseri
- CheckMate-77T (Nivolumab): FDA, 3 Ekim 2024’te seçilmiş rezektabl KHDAK hastalarında neoadjuvan nivolumab + platin bazlı kemoterapi ve cerrahi sonrası adjuvan nivolumab kullanımını onayladı.2
- KEYNOTE-671 (Pembrolizumab): FDA, 16 Ekim 2023’te rezektabl KHDAK için neoadjuvan pembrolizumab + platin bazlı kemoterapi ve cerrahi sonrası pembrolizumab devamı kullanımını onayladı.3
Mesane kanseri
- NIAGARA (Durvalumab): FDA, 28 Mart 2025’te kas invaziv mesane kanserinde neoadjuvan durvalumab + gemsitabin/sisplatin ve cerrahi sonrası adjuvan durvalumab kullanımını onayladı.4
- Pembrolizumab + enfortumab vedotin: Bu kombinasyonla ilgili perioperatif kullanım için güncel regulator kayıtları izlenmelidir. Bu yazıda, resmi kaynakla doğrulanmayan alt grup veya gelecek standart iddiaları kullanılmamıştır.
Mide kanseri
- MATTERHORN (Durvalumab): FDA, 25 Kasım 2025’te rezektabl mide veya gastroözofageal bileşke adenokarsinomunda durvalumab + FLOT’un neoadjuvan/adjuvan kullanımını onayladı. FDA özetinde olaydan bağımsız sağkalım için HR 0,71 bildirildi.5
Meme kanseri
- KEYNOTE-522 (Pembrolizumab): FDA, yüksek riskli erken evre üçlü negatif meme kanserinde neoadjuvan pembrolizumab + kemoterapi ve cerrahi sonrası adjuvan pembrolizumab kullanımını onaylamıştır.10 Türkiye’deki geri ödeme durumu ayrıca SGK/SUT üzerinden doğrulanmalıdır.
2. Yeni FDA Onayları ve Genişleyen Endikasyonlar
FDA’nın 2025 onkoloji onayları içinde immünoterapi ve hedefe yönelik tedavilerle ilgili birden fazla karar yer aldı. Aşağıdaki tablo, bu yazı kapsamında exact FDA sayfası ile doğrulanan örnekleri listeler.
Öne çıkan onaylar
| İlaç | Kanser Türü | Çalışma / kayıt | Yıl |
|---|---|---|---|
| Pembrolizumab + trastuzumab + kemoterapi | HER2+ mide/GEJ adenokarsinomu, PD-L1 CPS ≥1 | KEYNOTE-811 | 20258 |
| Durvalumab + FLOT | Rezektabl mide/GEJ adenokarsinomu | MATTERHORN | 20255 |
| Nivolumab + ipilimumab | Unrezektabl/metastatik MSI-H veya dMMR kolorektal kanser | FDA onay özeti | 20259 |
| Cemiplimab | Yüksek riskli kutanöz skuamöz hücreli karsinomda adjuvan tedavi | FDA onay özeti | 202511 |
Kolorektal kanserde dMMR/MSI-H alt grubu
DNA tamir mekanizması bozuk (dMMR) veya MSI-H kolorektal kanserlerde immünoterapi önemli bir araştırma ve tedavi alanıdır. FDA, 8 Nisan 2025’te nivolumab + ipilimumab kombinasyonunu unrezektabl veya metastatik MSI-H/dMMR kolorektal kanser için onayladı.9 Bu yazıda, henüz primer yayın veya regulator kayıtla doğrulanmayan kongre/medya iddiaları kullanılmamıştır.
3. Subkutan Formülasyonlar: Damar Yolu Yerine Cilt Altı Enjeksiyon

2025’in pratik yeniliklerinden biri, bazı immünoterapi ilaçlarının cilt altı (subkutan) enjeksiyon formunda onay almasıdır.6, 7
| Geleneksel (IV) | Subkutan (SC) |
|---|---|
| Damar yolundan infüzyon | Cilt altı enjeksiyon |
| Merkez protokolüne göre değişir | Uygulama süresi ürüne ve protokole göre değişir |
| Her seansta IV kanül takılır | İğne batışı ile tamamlanır |
| Hastanede bekleme süresi uzun | Daha kısa hastanede kalış |
- Pembrolizumab SC (Keytruda Qlex): FDA, 19 Eylül 2025’te IV pembrolizumab için onaylı solid tümör endikasyonlarında kullanılmak üzere subkutan pembrolizumab/berahyaluronidase alfa-pmph formunu onayladı.6
- Nivolumab SC (Opdivo Qvantig): FDA onaylı reçete bilgisinde nivolumab/hyaluronidase-nvhy formunun subkutan kullanım için onaylı olduğu belirtilir.7
Hasta için ne anlama geliyor? Cilt altı formlar bazı hastalarda uygulamayı kolaylaştırabilir. Türkiye’de ruhsat, temin ve geri ödeme durumu ayrıca Türkiye İlaç ve Tıbbi Cihaz Kurumu, SGK ve tedavi merkezi üzerinden doğrulanmalıdır.
4. Türkiye’de SGK Kapsamı: Nasıl Doğrulanmalı?

Türkiye’de immünoterapi geri ödemesi ilaç adı, kanser türü, evre, biyobelirteç sonucu, önceki tedaviler ve SUT kriterlerine göre değişir. SGK’nın bedeli ödenecek ilaçlar listesi ve duyuruları resmi doğrulama kaynağıdır.13
Doğrulama için pratik kontrol listesi:
- İlacın etkin maddesi ve ticari adı
- Kanser türü ve evre
- PD-L1, MSI-H/dMMR, HER2, BRCA gibi gerekli biyobelirteçler
- Önceki tedaviler ve progresyon durumu
- Güncel SUT ve SGK duyuru tarihi
Önemli: Bu yazı SGK geri ödeme garantisi vermez. Güncel durum için onkoloğunuza, hastane eczanesine ve resmi SGK/SUT kayıtlarına başvurunuz.13
5. Geleceğe Bakış: mRNA Kanser Aşıları ve Yapay Zeka

Kişiselleştirilmiş mRNA kanser aşıları
COVID-19 aşılarında kullanılan mRNA teknolojisi, kanser tedavisi araştırmalarında da değerlendirilmektedir.12
- Hastanın tümör DNA’sı analiz edilerek kişiye özel aşı hazırlanıyor
- Amaç: ameliyat sonrası kalan mikro düzeydeki kanser hücrelerine karşı bağışıklık yanıtı oluşturmak
- Pankreas kanseri ve bazı diğer tümörlerde erken faz çalışmalar yürütülmektedir; bu yaklaşımlar henüz standart tedavi anlamına gelmez.12
Yapay zeka ve biyobelirteçler
- Yapay zeka, ctDNA ve yeni biyobelirteçler immünoterapi yanıtını öngörme ve tedavi kararlarını kişiselleştirme amacıyla araştırılmaktadır.
- Bu alanlardaki sonuçlar kanser türüne, test yöntemine ve çalışmanın kalitesine göre değişir; klinik karar için tek başına yeterli kabul edilmemelidir.
Sonuç
2025-2026 dönemi, immünoterapinin bazı kanser türlerinde erken evre/perioperatif kullanıma doğru genişlediğini ve subkutan formların gündeme geldiğini gösteriyor. Ancak her gelişme her hasta için uygun değildir. Tedavi seçimi kanser türü, evre, biyobelirteçler, eşlik eden hastalıklar, ruhsat ve geri ödeme koşulları birlikte değerlendirilerek yapılmalıdır.
⚠️ Sorumluluk reddi: Bu blog yazısı genel bilgilendirme amaçlıdır. Tedavi kararları mutlaka onkoloğunuz tarafından verilmelidir. İlaç dozları ve tedavi şemaları burada paylaşılmamıştır.
Kaynaklar
- National Cancer Institute. Immunotherapy to Treat Cancer. https://www.cancer.gov/about-cancer/treatment/types/immunotherapy. Erişim: 2026-05-14.
- U.S. Food and Drug Administration. FDA approves neoadjuvant/adjuvant nivolumab for resectable non-small cell lung cancer. https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-neoadjuvantadjuvant-nivolumab-resectable-non-small-cell-lung-cancer. Erişim: 2026-05-14.
- U.S. Food and Drug Administration. FDA approves neoadjuvant/adjuvant pembrolizumab for resectable non-small cell lung cancer. https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-neoadjuvant-adjuvant-pembrolizumab-resectable-non-small-cell-lung-cancer. Erişim: 2026-05-14.
- U.S. Food and Drug Administration. FDA approves durvalumab for muscle invasive bladder cancer. https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-durvalumab-muscle-invasive-bladder-cancer. Erişim: 2026-05-14.
- U.S. Food and Drug Administration. FDA approves durvalumab for resectable gastric or gastroesophageal junction adenocarcinoma. https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-durvalumab-resectable-gastric-or-gastroesophageal-junction-adenocarcinoma. Erişim: 2026-05-14.
- U.S. Food and Drug Administration. FDA approves pembrolizumab and berahyaluronidase alfa-pmph for subcutaneous injection. https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-pembrolizumab-and-berahyaluronidase-alfa-pmph-subcutaneous-injection. Erişim: 2026-05-14.
- U.S. Food and Drug Administration. Opdivo Qvantig prescribing information. https://www.accessdata.fda.gov/drugsatfda_docs/label/2024/761429s000lbl.pdf. Erişim: 2026-05-14.
- U.S. Food and Drug Administration. FDA approves pembrolizumab for HER2 positive gastric or gastroesophageal junction adenocarcinoma expressing PD-L1 (CPS ≥1). https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-pembrolizumab-her2-positive-gastric-or-gastroesophageal-junction-adenocarcinoma. Erişim: 2026-05-14.
- U.S. Food and Drug Administration. FDA approves nivolumab with ipilimumab for unresectable or metastatic MSI-H or dMMR colorectal cancer. https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-nivolumab-ipilimumab-unresectable-or-metastatic-msi-h-or-dmmr-colorectal-cancer. Erişim: 2026-05-14.
- U.S. Food and Drug Administration. FDA approves pembrolizumab for high-risk early-stage triple-negative breast cancer. https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-pembrolizumab-high-risk-early-stage-triple-negative-breast-cancer. Erişim: 2026-05-14.
- U.S. Food and Drug Administration. FDA approves cemiplimab-rwlc for adjuvant treatment of cutaneous squamous cell carcinoma. https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-cemiplimab-rwlc-adjuvant-treatment-cutaneous-squamous-cell-carcinoma. Erişim: 2026-05-14.
- National Institutes of Health. An mRNA vaccine to treat pancreatic cancer. https://www.nih.gov/news-events/nih-research-matters/mrna-vaccine-treat-pancreatic-cancer. Erişim: 2026-05-14.
- Sosyal Güvenlik Kurumu. 2025/1. Dönem İlaç Geri Ödeme Komisyonu Kararlarına İstinaden Bedeli Ödenecek İlaçlar Listesinde Yapılan Düzenlemeler Hakkında Duyuru. https://www.sgk.gov.tr/Duyuru/Detay/20251-Donem-Ilac-Geri-Odeme-Komisyonu-Kararlarina-Istinaden-Bedeli-Odenecek-Ilaclar-Listesinde-Yapilan-Duzenlemeler-Hakkinda-Duyuru-2025-09-16-10-01-39. Erişim: 2026-05-14.
